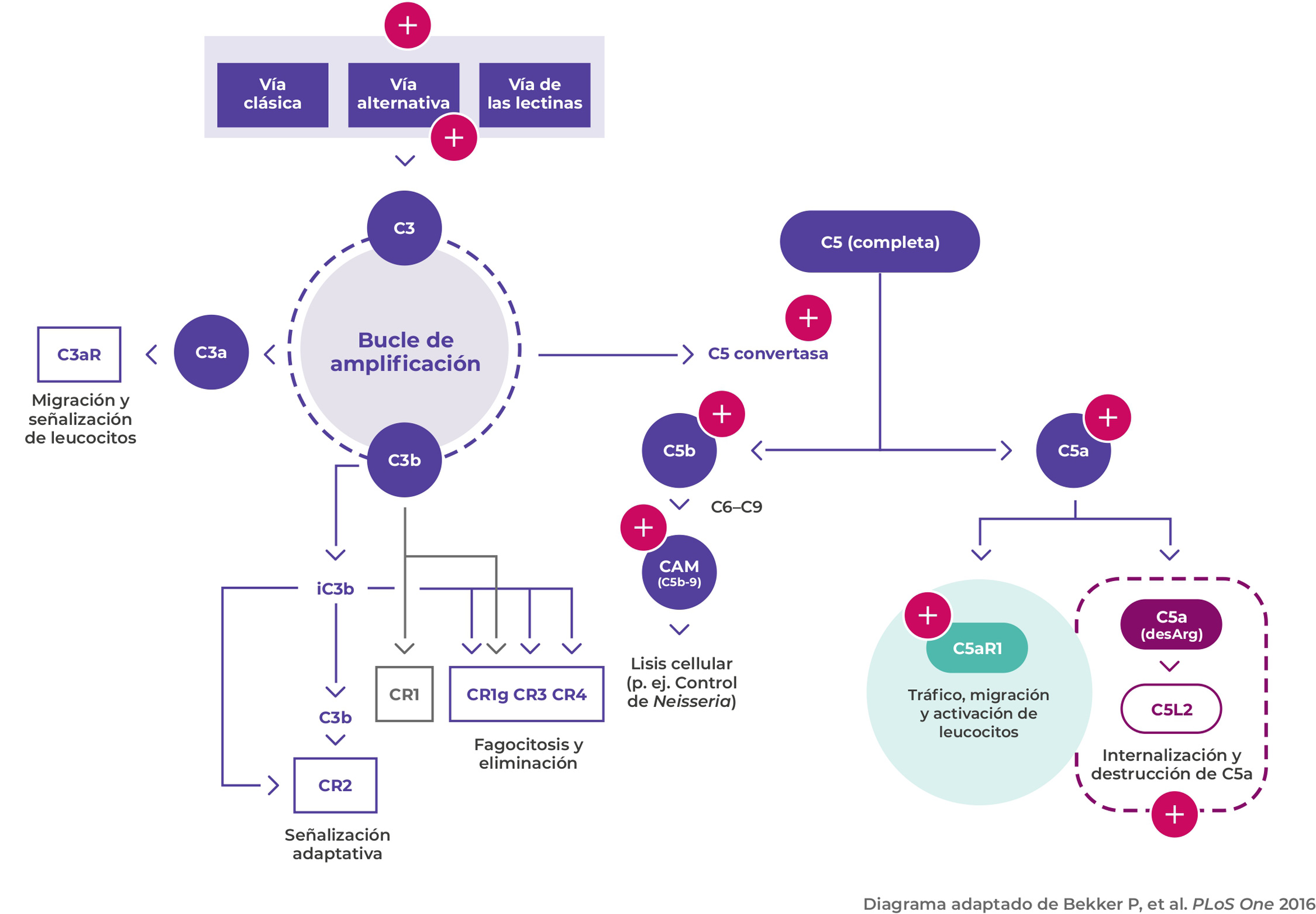
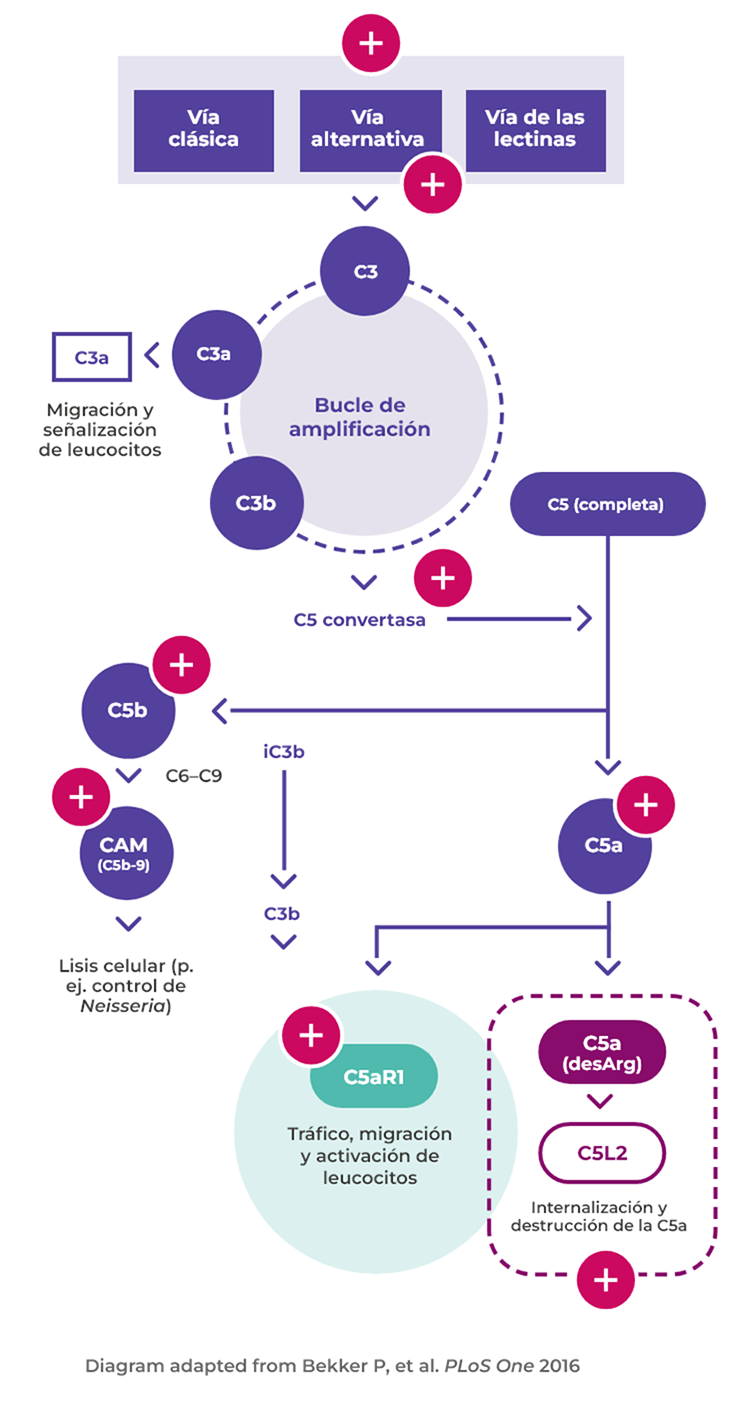
Patogenia de la VAA
El desarrollo de VAA es un proceso autoinmune complejo y multifactorial2,3
En la actualidad, no están claras las causas iniciales de la VAA2,3 Factores predisponentes como una infección microbiana, la influencia genética, los agentes ambientales y ciertos medicamentos son fundamentales para el desarrollo de la VAA.2,3
La exposición al sílice, pesticidas, humos, materiales de construcción, hidrocarburos (agentes limpiadores, pintura, diésel), fármacos (propiltiouracilo, hidralazina, D-penicilamina, cefotaxima, minociclina, agentes anti-TNF, fenitoína) y ciertas sustancias psicoactivas puede causar VAA.2,3
Aparición de ANCA
Pérdida de tolerancia inmunológica a los antígenos de ANCA y producción de ANCA por parte de las células plasmáticas1
Normalmente, los ANCA se dirigen a las enzimas lisosómicas PR3 y MPO de los neutrófilos en la GPA (granulomatosis con poliangeítis, anteriormente denominada granulomatosis de Wegener) y la PAM (poliangeítis microscópica), respectivamente1-5
Preactivación de los neutrófilos
Las citocinas inflamatorias (TNF-α, IL-1 e IL-18), que se liberan como respuesta a una infección u otro acontecimiento, siendo relevante también la predisposición genética, preactivan los neutrófilos2,6,7
Exposición de antígenos de ANCA
En la superficie de los neutrófilos preactivados aparecen los antígenos de ANCA (p. ej. MPO y PR3), que pueden ser reconocidos por los ANCA causando la activación del neutrófilo1,2,6,7
Liberación de mediadores inflamatorios
Los neutrófilos activados se adhieren y penetran en la pared de los vasos sanguíneos y liberan mediadores de la inflamación y del daño celular, p. ej. NET1,2,6
Activación del complemento por vía alternativa
Los neutrófilos activados liberan además factores, como la properdina, que tienen un papel autocrino en la activación del complemento por vía alternativa y conducen a la generación de C5a1,6
Unión de C5a a C5aR1
La unión de C5a al C5aR1 amplifica la inflamación y el daño vascular causados por los ANCA6
Vasculitis necrosante
Este proceso conduce a la vasculitis necrosante de los vasos sanguíneos pequeños6
Inflamación crónica
En unos días, la inflamación aguda y la necrosis son reemplazadas por la inflamación crónica y la cicatrización6
La importancia del complemento y los neutrófilos en la activación de la VAA
C5a tiene un papel fundamental en la patogenia de la VAA, al amplificar la inflamación y el daño vascular causados por los ANCA1

Introducción a la VAA
La VAA es un tipo de vasculitis de pequeño vaso, es una enfermedad rara y grave, que afecta a múltiples órganos y presenta un riesgo elevado de mortalidad1
Seguir leyendo
Mecanismo de la enfermedad
La activación del complemento por la vía alternativa y la interacción entre los neutrófilos y C5a es clave en el daño vascular en la VAA2
Seguir leyendo
Tratamiento de las VAA
Un marco para el tratamiento en la práctica clínica y el control de pacientes con VAA
Seguir leyendo